Saat kita menulis di papan tulis menggunakan spidol, sejatinya kita akan mencium bau khas dari spidol. Penggambaran atas akasus tersebut hakikatnya merupakan senyawa kimia yaitu toluena yang juga sering digunakan dalam cat tembok.
Toluena juga memiliki kegunaan yang lebih banyak daripada yang kita pikirkan. Salah satu bahan kimia yang banyak digunakan baik dalam kehidupan sehari hari maupun dalam kimia industri.
Toluena
Senyawa benzena atau senyawa aromatik menjadi suatu senyawa kimia organik yang sangat fleksibel. Dalam artian yaitu bahwa senyawa aromatik tersebut dapat memiliki senyawa turunan yang sangat beragam.
Hal itu karena kemungkinan reaksi yang sangat banyak dimiliki oleh senyawa benzena sehingga mampu mengikat berbagai gugus fungsi. Toluena menjadi salah satu turunan senyawa aromatik benzena yang juga dikenal dengan metil benzena.
Pengertian Toluena
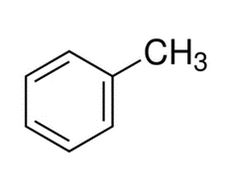
Toluena adalah sebuah senyawa aromatis benzena yang mengikat satu buah gugus metil (-CH3) dalam cincinnya dimana gugus metil ini menggantikan salah satu atom hidrogen pada benzena dengan rumus kimia C7H8. Adanya gugus metil yang terikat dalam sebuah benzena itu yang membuat toluena juga memiliki nama metil benzena.
Sehingga toluena atau yang juga dikenal dengan toluol merupakan sebuah senyawa kimia hidrokarbon aromatik. Senyawa ini juga memiliki nama lain seperti metil benzena, anisen, dan fenil metana.
Toluena menjadi senyawa yang banyak digunakan sebagai material awal dalam industri manufaktur kimia. Toluena terdapat dalam minyak bumi dalam jumlah minor dan juga terdapat dalam batu bara dengan kadar 15 sampai dengan 20 %.
Kedua sumber tersebut menyediakan toluena sebagai penggunaan komersial, namun toluena dalam jumlah yang lebih banyak diproduksi secara sintesis katalitik dari petroleum naphtha.
Pengertian Toluena Menurut Para Ahli
Adapun definisi toluena menurut para ahli, antara lain;
- Rumalutur (2018), Toluena adalah bagian pelarut yang dimanfaatkan dalam kehidupan manusia termasuk menjadi menjadi bahan pencampur bensin bersama dengan benzena dan xilena.
Sifat Fisika Toluena
Toluena memiliki bentuk liquid atau cairan yang tidak berwarna atau bening. Senyawa ini memiliki aroma yang tajam dan sangat mudah terbakar. Jika dibandingkan dengan air, toluena memiliki densitas yang lebih rendah daripada air yakni sebesar 867 kg/m3.
Sifat kelarutannya dalam air yakni sedikit larut dalam air karena senyawa ini termasuk dalam golongan senyawa hidrokarbon sehingga kepolarannya cenderung rendah. Hal itulah yang membuat toluena tidak akan bercampur dalam air dan akan membentuk dua lapisan.
Selayaknya minyak yang dicampur dengan air, toluena akan membentuk dua lapisan jika berada dalam air. Toluena akan berada di atas air karena memiliki densitas atau massa jenis yang lebih rendah dibandingkan dengan air. Sifat toluena ini sedikit mirip dengan minyak karena memang berasal dari minyak bumi.
Sifat Kimia Toluena
Reaksi kimia dari toluena memiliki karakteristik yang mirip dengan reaksi normal dari senyawa hidrokarbon aromatik dalam substitusi elektrofilik aromatik. Hal ini disebabkan karena gugus metil yang ada di senyawa tolena memiliki sifat pelepasan elektron yang lebih baik dibandingkan ketika mengikat hidrogen dalam posisi yang sama.
Dengan kata lain, gugus metil bersifat pendorong atau donor elektron bagi senyawa aromatiknya. Gugus metil ini memiliki reaktivitas yang lebih tinggi jika dibandingkan dengan benzena dengan suatu elektrofil. Reaksi yang dapat terjadi seperti sulfonasi untuk menghasilkan asam p-toluena sulfonat dan juga klorinasi dengan Cl2 dengan keberadaan FeCl2 untuk menghasilkan senyawa para dan orto dari isomer kloro toluena.
Hal penting lainnya yakni gugus metil pada toluena juga sangat mudah mengalami oksidasi. Ini dapat terjadi ketika terdapat kalium permanganat sehingga akan menghasilkan produk akhir yakni asam benzoat atau bereaksi dengan kromil klorida menghasilkan benzaldehida.
Dalam kondisi radikal bebas, gugus metil ini juga akan mengalami reaksi halogenasi. Sebagai contoh yaitu N-bromo siccinimide (NBS) ketika dipanaskan dengan toluena dengan keberadaan senyawa inisiator AIBN akan menghasilkan produk benzil bromida.
Senyawa AIBN sebagai inisiator akan menginisiasi toluena dalam membentuk senyawa radikal. Selain dengan inisiator tersebut, toluena juga dapat mengalami brominasi dengan HBr dan H2O2 dengan adanya inisiator cahaya.
Namun demikian toluena juga memiliki dampak negatif jika terpapar secara berlebihan dalam tubuh kita. Meskipun tidak diklasifikasikan sebagai senyawa karsinogenik, namun toluena memiliki efek lain bagi manusia.
Efek tersebut terjadi ketika kita terpapar toluena dalam waktu yang lama dimana akan mengganggu fungsi ginjal, jantung, hati, otak, dan juga sistem saraf manusia.
Oleh karena itu sebaiknya kita sebisa mungkin menghindari ataupun mengurangi penggunaan produk yang mengandung toluena. Namun jika terpaksa untuk menggunakan sebaiknya gunakan dengan bijak dan dengan prosedur keamaan sehingga tidak membuat kita terpapar oleh senyawa toluena secara berlebih.
Tahapan Proses Pembuatan Toluena
Adapun sistem dalam pembuatan toluena, antara lain sebagai berikut;
-
Sintesis Toluena
Pembuatan toluena dapat dilakukan secara sintesis di laboratorium yang juga diimplementasikan pada industri bahan kimia.
Pembuatannya tentu menggunakan bahan awal benzena sebagai penyedia senyawa aromatis dan juga metil klorida sebagai penyedia gugus metil. Benzena akan bereaksi dengan metil klorida dengan keberadaan asam lewis seperti aluminium klorida untuk menghasilkan toluena.
C6H6 + CH3Cl → C6H5CH3 + HCl
Selain dari bahan metil klorida, toluena juga dapat disintesis dengan benzena dan juga metanol melalui reaksi alkilasi benzena. Dalam reaksi ini terjadi pelepasan molekul air dimana benzena yang melepas ion H+ sedangkan metanol yang melepaskan ion hidroksida.
C6H6 + CH3OH → C6H5CH3 + H2O
-
Sintesis Toluena dari Batu Bara
Seperti yang telah kita singgung sebelumnya bahwa batu bara juga menjadi salah satu sumber toluena. Tar batu bara biasa digunakan oleh industri sebagai sumber dalam pembuatan toluena. Fraksi minyak bumi ringan dari tar batu bara adalah bagian yang sering digunakan secara komersial.
Minyak ini akan dibersihkan dengan menggunakan asam sulfat untuk menghilangkan senyawa basa yang ada dalam minya.
Kemudian akan dibilas lagi dengan menggunakan basa natrium hidroksida untuk menghilangkan senyawa asam dalam minyak tersebut dalam hal ini yakni asam sulfat. Pada tahap terakhir, pembilasan dilakukan dengan menggunakan air.
Reaksi Toluena
Penjelasan terkait reaksi toluena, antara lain;
-
Oksidasi Toluena
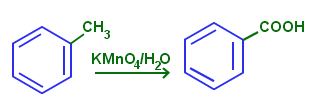
Sebagai senyawa aromatik, toluena akan lebih mudah mengalami reaksi oksidasi. Gugus metil dalam senyawa aromatik ini akan mudah teroksidasi menjadi gugus karboksil dengan keberadaan agen oksidator kuat. Oksidasi toluena ini akan menghasilkan senyawa benzaldehida yang dapat dioksidasi lebih lanjut menghasilkan asam benzoat. Salah satu jenis agen oksidator yang biasa digunakan adalah kalium permanganat.
-
Brominasi Toluena
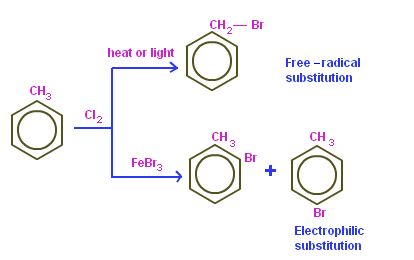
Reaksi selanjutnya dalam toluena yaitu reaksi brominasi yang termasuk dalam reaksi halogenasi. Brominasi dapat terjadi pada salah satu karbon dalam cincin aromatis toluena ataupun terjadi pada gugus metil toluena. Reaksi brominasi ini memiliki dua jenis mekanisme yang berbeda yakni melalui adanya sisi radikal pada gugus metil ataupun melalui substitusi elektrofilik pada cincin aromatik.
Adanya gugus radikal yang terjadi pada gugus metil dengan inisiator tertentu akan menyebabkan reaksi brominasi terjadi pada gugus metil. Dalam hal ini berarti bromin akan terikat pada gugus CH3 dan gugus tersebut akan berubah menjadi -CH2-Br.
Namun ketika reaksi terjadi secara substitusi elektrofilik maka bromin akan terikat pada salah satu atom karbon dalam gugus aromatik.
Kegunaan Toluena
Manfaat yang bisa di dapatkan dalam toluena, yaitu;
-
Dalam Kimia Industri
Toluena banyak digunakan dalam bidang kimia laboratorium ataupun industri sebagai pelarut. Dengan sifat yang dimiliki yakni non polar membuat senyawa ini digunakan sebagai pelarut organik atau pelarut non polar. Selain itu, toluena juga biasa digunakan sebagai prekursor dalam reaksi substitusi ataupun oksidasi untuk menghasilkan produk senyawa kimia tertentu.
-
Dalam Cat
Toluena banyak digunakan dalam campuran cat, tinta spidol, ataupun thinner. Peran toluena dalam produk tersebut ialah sebagai pelarut.
Toluena mampu melarutkan berbagai senyawa penyusun cat ataupun spidol seperti pigmen warna dan elemen lainnya sehingga dapat bercampur menjadi larutan yang homogen. Namun dalam aplikasinya, toluena akan menguap sehingga membuat cat menjadi kering setelah diaplikasikan.
-
Bahan Peledak
Toluena juga banyak digunakan sebagai prekursor dalam pembuatan bahan peledak. Sebenarnya bukan secara langsung toluena yang digunakan sebagai bahan peledak melainkan akan dilakukan sintesis senyawa trinitrotoluena dari bahan toluena ini.
Senyawa trinitrotoluena atau dikenal dengan TNT ini merupakan senyaw toluena yang mengikat tiga gugus lain yakni gugus nitro dalam cincin aromatiknya. TNT dikenal memiliki daya ledak yang sangat besar atau bersifat sangat eksplosif. Hal itu yang membuat TNT banyak digunakan sebagai bahan peledak sejak perang dunia 2.
Demikian artikel lengkap yang bisa kami berikan bahasan tentang pengertian toluena menurut para ahli, sifat, tahapan proses, reaksi, dan kegunaannya dalam kehidupan sehari-hari. Semoga melalui tulisan ini dapat membantu dan bermanfaat bagi segenap pembaca yang membutuhkannya.