
Ikatan kimia akan senantisa terjadi karena setiap unsur mempunyai salah satu kemampuan dasar yang dimiliki yaitu atom untuk berinteraksi dengan unsur atom yang lain. Terjadinya ikatan kimia ini sangatlah dipengaruhi oleh keberadaan elektron dalam atom.
Dimana elektron memiliki peranan yang sangat besar dalam terbentuknya ikatan kimia. Selain itu, ikatan kimia juga dibedakan dalam beberapa jenis yang didasarkan pada bagaimana mekanisme unsur untuk saling membetuk ikatan kimia.
Ikatan Kimia
Dalam kehidupan di bumi, sejatinya setiap manusia sangat bergantung terhadap berbagai zat salah satunya yaitu air (H2O) yang merupakan penyusun utama tubuh manusia. Selain itu, manusia juga membutuhkan zat lain seperti makanan, garam (NaCl), dan material lainnya. Namun yang pasti, tidak akan pernah menemukan zat tersebut seperti H2O maupun NaCl di dalam tabel periodik unsur. Dengan wujud gambar sebagai berikut;
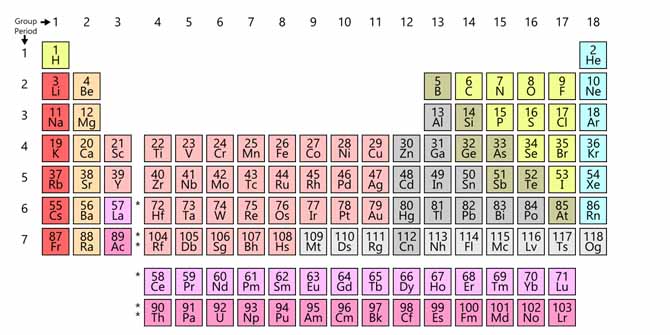
Penjelasan atas hal tersebut yaitu karena tabel periodik hanya mengatur sebanyak 118 jenis unsur kimia yang dikenal saat ini, sedangkan air dan garam bukan merupakan unsur melainkan senyawa. Senyawa merupakan hasil gabungan dari beberapa unsur dengan perbandingan rasio tetap.
Seperti halnya air atau H2O yang terdiri dari dua unsur hidrogen dan satu oksigen, begitu pula garam yang terdiri dari satu unsur natrium dan klorida. Suatu unsur dapat membentuk senyawa karena mereka memiliki kemampuan untuk saling membentuk ikatan yang disebut ikatan kimia.
Adapun dalam sejarahnya, gagasan tentang ikatan kimia muncul pada awal abad ke-20 dimana pada saat tersebut telah ditemukan teori mekanika kuantum untuk mendeskripsikan perilaku elektron dalam atom. Para ahli kimia membutuhkan persamaan mekanika bilangan kuantum yang sangat rinci untuk mencapai pemahaman tentang pembentukan ikatan kimia.
Pengertian Ikatan Kimia
Ikatan kimia adalah interaksi yang berperan dalam menyatukan dan menghubungkan satu atom dengan atom lain dalam membentuk molekul, ion, kristal, dan spesi lain untuk mencapai kestabilan, sehingga dalam hal ini terdapat dua atom yang saling mendekat, maka inti atom dan elektronnya akan berinteraksi dan akan cenderung mendistribusikan diri sedemikian rupa sehingga mencapai energi yang lebih rendah atau berarti mencapai kestabilan yang tinggi karena tingkat energi berbanding terbalik dengan kestabilan.
Bahkan ketika energi total dari gabungan atom lebih rendah daripada energi masing masing atom, maka mereka akan berikatan bersama sehingga menyebabkan penurunan energi yang disebut dengan energi ikatan.
Pengertian Ikatan Kimia Menurut Para Ahli
Adapun definisi ikatan kimia menurut para ahli, antara lain;
- Irfan Anshory (2000), Ikatan kimia adalah cabang ilmu pengetahuan alam yang mempelajari tentang struktur materi, sifat-sifat materi, perubahan suatu materi menjadi materi lain, serta energi yang menyertai perubahan materi.
- Agung Nugroho Catur Saputro & Irwan Nugraha (2008), Definisi ikatan kimia ialah ilmu pengetahuan alam yang mengkaji tentang materi yang meliputi struktur, susunan, sifat, dan perubahan materi serta energi yang menyertainya.
Jenis Ikatan Kimia
Adapun untuk macam-macam ikatan kimia, antara lain;
Sesuai dengan namanya, ikatan kovalen yang terdiri dari “co” yang berarti gabungan sedangkan “valent” yang berarti valensi merupakan ikatan kimia yang melibatkan atom-atom untuk saling berikatan menghasilkan tingkat energi terendah dan stabilitas tertinggi dimana elektron valensi digunakan sebagai media berikatan antar atom tersebut.
Dalam ikatan kovalen, interaksi yang terjadi yaitu pembagian pasangan elektron antara dua atom yang saling berikatan dimana pasangan elektron tersebut merupakan hasil penggabungan elektron valensi dua atom yang saling berikatan. Ikatan kovalen dapat terjadi pada dua atom ataupun dalam beberapa atom sekaligus dalam membentuk suatu senyawa.
Berdasarkan kekuatan ikatannya, ikatan kovalen dapat dibedakan menjadi beberapa jenis:
- Ikatan Kovalen Tunggal
Ikatan kovalen tunggal merupakan ikatan yang terbentuk dengan adanya dua atom yang berbagi satu buah elektronnya untuk membentuk ikatan.
Ikatan tunggal dapat digambarkan dengan simbol garis tunggal. Ikatan ini memiliki kekuatan yang paling lemah karena hanya memiliki satu buah ikatan dari hanya satu elektron yang berinteraksi. Contoh ikatan ini yaitu HCl, H2O, H2.
- Ikatan Kovalen Rangkap Dua
Ikatan kovalen rangkap dua merupakan ikatan kovalen yang terbentuk dengan adanya dua atom yang berbagi dua buah elektronnya dalam membentuk ikatan.
Ikatan rangkap dua dapat digambarkan dengan simbol garis ganda. Jenis ikatan ini memiliki kekuatan yang lebih tinggi dibandingkan ikatan tunggal karena memiliki dua buah elektron yang berinteraksi. Contoh senyawa dengan ikatan ini yaitu O2.
- Ikatan Kovalen Rangkap Tiga
Jenis ikatan kovalen rangkap tiga terbentuk oleh adanya tiga buah elektron yang digunakan untuk berbagi oleh dua atom.
Ikatan ini dapat digambarkan sebagai yaitu garis rangkap tiga. Jenis ikatan rangkap tiga merupakan ikatan kovalen yang paling kuat karena memiliki tiga buah elektron untuk digunakan. Contoh senyawa dengan ikatan ini yaitu N2.
Berdasarkan kepolarannya, ikatan kovalen dapat dibagi menjadi 2 jenis:
- Ikatan Kovalen Polar
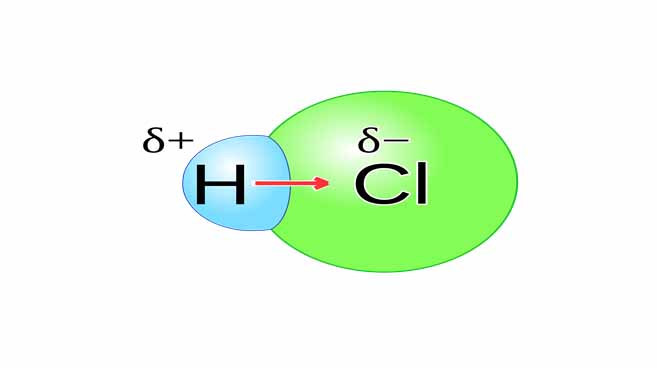
Ikatan kovalen polar merupakan ikatan kovalen yang terjadi antar atom yang memiliki nilai elektronegativitas yang berbeda. Sebagai contoh yaitu pada HCl dimana H memiliki elektronegativitas rendah yaitu bermuatan parsial positif sedangkan Cl memiliki elektronegativitas tinggi bermuatan parsial negatif sehingga HCl dapat dikatakan sebagai ikatan kovalen polar.
Dalam kovalen polar, elektron yang digunakan bersama-sama akan cenderung mengarah ke salah satu atom yang memiliki elektronegativitas lebih tinggi. Pada HCl, elektron dari H akan lebih tertarik ke arah atom Cl.
 Ikatan Kovalen Nonpolar
Ikatan Kovalen Nonpolar
Ikatan kovalen nonpolar merupakan ikatan yang terjadi antar atom yang tidak memiliki beda elektronegativitas. Contoh ikatan ini yaitu terjadi pada senyawa H2 dimana antara kedua hidrogen yang berikatan memiliki elektronegativitas yang sama sehingga ikatan ini disebut kovalen nonpolar.
Sifat-sifat senyawa dengan ikatan kovalen:
- Senyawa dengan ikatan kovalen memiliki titik didih dan titik lebur yang rendah
- Senyawa tidak mampu menghantar listrik
- Kovalen polar dalam bentuk larutan mampu menghantarkan listrik
- Senyawa kovalen pada umumnya tidak larut dalam air
- Senyawa kovalen dapat larut dalam pelarut nonpolar
Ikatan ionik adalah ikatan yang terjadi antara atom yang melepaskan elektron dengan atom yang menerima elektron. Dalam ikatan ionik dikenal kation dan anion, kation merupakan atom yang bermuatan positif sedangkan anion merupakan atom yang bermuatan negatif. Atom yang kehilangan elektron akan bermuatan positif sedangkan atom yang menerima elektron akan bermuatan negatif.
Adanya perbedaan muatan tersebut akan menyebabkan gaya tarik menarik yang merupakan interaksi ikatan dari kedua atom yang saling berikatan. Ikatan ionik biasanya terjadi antara atom golongan IA dan IIA dengan VIA dan VIIA.
Contoh dari ikatan ionik yaitu terdapat pada senyawa KCl. Atom kalium (K) yang memiliki 19 elektron akan melepaskan satu elektron terluarnya sehingga hanya memiliki 18 elektron menjadi bermuatan positif (K+) sedangkan Cl yang memiliki 17 elektron akan menerima satu elektron dari K sehingga menjadi 18 elektron dan bermuatan negatif (Cl–).
Perbedaan muatan antara K+ dengan Cl– akan menyebabkan kedua atom ini saling tarik menarik dan menghasilkan kekuatan ikatan.
Sifat sifat senyawa dengan ikatan ionik:
- Senyawa memiliki titik didih dan titik lebur yang cukup tinggi
- Leburan dan larutan dari senyawa ionik mampu menghantarkan listri
- Sifat mekanik senyawa ini yaitu mudah patah
- Senyawa ionik mudah larut dalam air melalui proses solvasi
- Senyawa ionik tidak dapat larut dalam pelarut nonpolar karena penyusun senyawa ini hanya berupa senyawa polar.
-
Ikatan Logam/Metalik
Ikatan logam adalah jenis ikatan kimia yang terbentuk akibat adanya gaya tarik elektrostatik antara elektron dalam bentuk awan elektron dengan ion logam lain yang bermuatan positif. Ikatan ini dapat digambarkan sebagai pembagian elektron bebas dalam suatu kation.
Suatu logam memiliki elektronegativitas yang rendah dan mudah terionisasi serta kehilangan elektron valensinya. Elektron yang dilepas akan membentuk awan elektron disekitar ion menghasilkan gaya elektrostatik. Kation logam yang dikelilingi elektron dikenal dengan istilah lautan elektron.
Sifat-sifat senyawa dengan ikatan logam:
- Senyawanya mudah menghantarkan listrik
- Sifat mekanik senyawa ini ulet dan mudah dibentuk
- Kekuatan tinggi
- Memiliki ketahanan suhu tinggi
Contoh Soal Ikatan Kimia
Adapun untuk beberapa contoh soal dan jawaban yang ada dalam ikatan kimia ini, antara lain;
- Berikut ini yang merupakan senyawa dengan ikatan kovalen polar adalah…
| a. N2 | b. NaCl |
| c. KBr | d. HBr |
HBr terdiri dari hidrogen dengan muatan parsial positif (elektronegativitas rendah) dan Br dengan muatan parsial negatif (elektronegativitas tinggi).
- Diantara senyawa berikut mana yang paling polar….
| a. HCl | b. HF |
| c. Cl2 | d. HBr |
Selisih elektronegativitas hidrogen (H) dengan fluorin (F) paling tinggi
- Berikut ini manakah yang memiliki ikatan kovalen rangkap dua….
| a. C2H4 | b. CH4 |
| c. HCl | d. NaOH |
C2H4 terdiri dari satu buah ikatan rangkap dua antara C=C dan empat buah ikatan tunggal C-H
- Manakah senyawa berikut yang memiliki kekuatan ikatan paling rendah….
| a. CH4 | b. O2 |
| c. H2 | d. N2 |
CH4 hanya memiliki ikatan tunggal sehingga kekuatannya rendah
- Jenis ikatan apa yang terjadi antara atom 17X dengan 19Y …..
| a. Kovalen polar | b. Ionik |
| c. Logam | d. Kovalen nonpolar |
Atom X yaitu Cl sedangkan atom Y yaitu K sehingga berikatan secara ionik membentuk KCl
Dari penjelasan yang dikemukakan, dapatlah dikatakan bahwa adanya ikatan kimia memungkinkan terbentuknya jutaan senyawa baru yang merupakan kombinasi dari berbagai atom. Terbentuknya ikatan kimia sangat ditentukan oleh perilaku dan sifat dari elektron terluar atau elektron valensi suatu atom.
Hal tersebut dikarenakan elektron valensi dari suatu atom akan berinteraksi dengan elektron valensi atom lain untuk suatu membentuk ikatan kimia. Terbentuknya suatu ikatan kimia yang baru menandakan bahwa telah terjadi suatu reaksi kimia.
Disisi lain, untuk interaksi antar atom dan ikatan kimia dapat diklasifikasikan ke dalam beberapa macam yang berbeda dimana hal tersebut didasarkan pada bagaimana cara suatu atom saling berinteraksi satu sama lain dalam membentuk ikatan. Pada dasarnya ikatan kimia dibedakan menjadi dua jenis yaitu ikatan kovalen, ikatan ionik, dan juga ikatan logam atau metalik.
Itulah tadi pembahasan serta penjelasan mengenai pengertian ikatan kimia, macam, contoh soalnya dan jawabannya. Semoga artikel ini bisa memberikan wawasan kepada segenap pembaca, terutama yang sedang mencari materinya.


